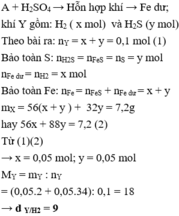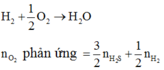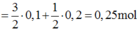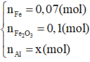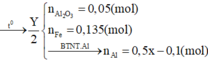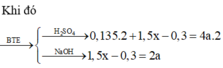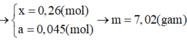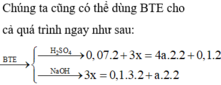cho 46,4g hỗn hợp X\(\left\{{}\begin{matrix}Fe\\S\end{matrix}\right.\)=to> hỗn hợp Y tác dụng với H2SO4 loãng thu được 13,44 l hỗn hợp khí. biết các phản ứng xảy ra hoàn toàn
a) tính %m hỗn hợp X
b) nếu dẫn 13,44l hỗn hợp khí trên vào dd CuSO4 dư thu được m (g) kết tủa. Xác định m